Pengertian Materi
Materi adalah sesuatu yang memiliki massa dan juga menempati ruang. Menurut kalian, apa sih contoh materi itu?
Misalnya, kayu, batu, air, gas, dan masih banyak lainnya.
Nah, berdasarkan wujudnya materi itu dibagi menjadi tiga, yaitu zat padat, cair, dan gas.
Setiap zat memiliki karakteristik dan sifat yang berbeda. Berikut ini perbedaannya.
1. Zat padat
- Bentuk dan volumenya tetap
- Susunan jarak antarpartikelnya sangat rapat
- Partikel penyusunnya tidak dapat bergerak secara bebas
2. Zat cair
- Bentuknya berubah-ubah sesuai wadahnya dan volumenya tetap
- Susunan jarak antarpartikelnya agak renggang
- Partikel penyusunnya bisa bergerak secara terbatas
3. Gas
- Bentuk dan volumenya berubah-ubah
- Susunan jarak antarpartikelnya sangat renggan atau berjauhan
- Partikel penyusunnya bisa bebas bergerak
Klasifikasi Materi
Klasifikasi materi tersebut dapat dikatakan sebagai pengelompokan berdasarkan sifat fisika. Klasifikasi materi juga dapat dilakukan berdasarkan sifat kimia, yaitu komposisi partikel penyusunnya. Berdasarkan komposisinya, materi dapat dikelompokkan menjadi zat tunggal dan campuran. Materi yang termasuk ke dalam zat tunggal dibedakan lagi menjadi unsur dan senyawa.. Lantas, apa perbedaan keduanya?
1. Tunggal
Zat tunggal terdiri dari unsur dan molekul. Berikut penjabaran lengkapnya ya, .
a. Unsur
Bagian terkecil dari materi yang sudah tidak bisa diuraikan lagi menjadi materi lain yang lebih sederhana dengan reaksi kimia biasa.
Unsur disusun oleh atom-atom yang sejenis. Contoh unsur adalah O (oksigen), C (karbon), Ag (perak), Hg (merkuri), dan sebagainya.
Dalam penamaan unsur harus mengikuti aturan Berzelius berikut.
- Dinyatakan dalam satu huruf kapital, misalnya N (nitrogen), C (karbon), O (oksigen), dan sebagainya.
- Dinyatakan dalam dua huruf di mana huruf pertama harus kapital, contoh Ba (barium), Cr (kromium), Au (aurum), dan sebagainya.
- Dinyatakan dalam dua huruf di mana huruf pertama kapital dan huruf keduanya huruf khas, misalnya Zn (seng), Hg (merkuri), Mg (magnesium), Mn (mangan), dan sebagainya.
- Dinyatakan dalam tiga huruf di mana huruf pertamanya harus kapital, misalnya Uut (ununtrium).
Berdasarkan sifatnya, unsur dibagi menjadi tiga yaitu unsur logam, nonlogam, dan semilogam. Pembagian tersebut didasarkan pada kemiripan sifat-sifat unsurnya.
Untuk lebih jelasnya, kamu bisa lihat di sistem periodik unsur, ya.
b. Molekul
Kumpulan atom yang saling berikatan. Molekul dibagi menjadi dua, yaitu molekul unsur dan molekul senyawa.
- Molekul unsur adalah molekul yang tersusun oleh unsur-unsur sejenis. Artinya, molekul unsur memuat ikatan atom-atom sejenis. Contohnya O2 (gas oksigen) yang tersusun atas atom-atom O (oksigen).
- Molekul senyawa adalah molekul yang tersusun oleh unsur-unsur yang tidak sejenis. Artinya, molekul senyawa memuat ikatan atom-atom yang tidak sejenis. Contohnya CO2 (gas karbondioksida) yang tersusun atas atom C (karbon) dan O (oksigen).
2. Campuran
Campuran adalah materi yang dibentuk oleh dua zat atau lebih di mana sifat penyusun masing-masing zatnya tidak berubah.
Contoh campuran adalah larutan gula, susu, udara, dan sebagainya.
Adapun ciri-ciri campuran adalah sebagai berikut.
- Terbentuk dari dua zat atau lebih
- Sifat campuran sama dengan sifat zat penyusunnya
- Komposisi zat penyusunnya tidak tetap
- Zat-zat penyusunnya masih bisa dipisahkan kembali secara fisika
Menurut kelarutannya, campuran dibagi menjadi dua yaitu campuran homogen dan heterogen.
a. Campuran homogen
Disebut juga larutan adalah campuran yang zat terlarutnya bisa larut sempurna di dalam pelarut. Campuran ini dicirikan dengan terbentuknya larutan bening. Contohnya larutan gula.
Larutan atau campuran homogen ini dibagi menjadi tiga macam, yaitu larutan asam, basa, dan garam.
Untuk mendeteksi suatu larutan itu bersifat asam atau basa, dibutuhkan suatu indikator yang disebut indikator asam basa.
b. Campuran heterogen
Merupakan campuran yang zat terlarutnya tidak larut sempurna di dalam pelarut. Cirinya adalah terbentuknya endapan, cairan berwarna keruh, dan tidak tembus cahaya.
Contoh campuran heterogen adalah susu, pasir yang dilarutkan dalam air, dan sebagainya.
Zat penyusun pada campuran heterogen masih bisa dipisahkan secara fisika, misalnya melalui filtrasi, sentrifugasi, distilasi, kromatografi, sublimasi, dan evaporasi.
Apakah perbedaan istilah-istilah tersebut?
- Filtrasi adalah teknik penyaringan untuk memisahkan zat terlarut dan pelarut. Misalnya, filtrasi untuk memisahkan pasir dan air.
- Sentrifugasi adalah teknik pemisahan untuk zat pelarut yang berukuran sangat kecil dengan perbedaan massa jenis besar. Zat yang massa jenisnya besar akan mengendap di bawah.
- Distilasi adalah teknik pemisahan campuran menggunakan perbedaan titik didih dua zat. Zat yang memiliki titik didih rendah akan menguap terlebih dahulu, sehingga menyisakan zat yang titik didihnya lebih tinggi. Contohnya pada destilasi aseton dan air.
- Kromatografi adalah teknik pemisahan campuran berdasarkan perbedaan indeks bias cahaya.
- Sublimasi adalah teknik pemisahan campuran berdasarkan kecepatan zat untuk menyublim. Contohnya pada pemisahan kapur barus dan pasir.
- Evaporasi adalah teknik pemisahan campuran dengan menguapkan pelarutnya. Akibatnya, zat terlarutnya akan mengkristal.
Indikator Asam Basa
Pada pembahasan sebelumnya, sudah dikenalkan dengan indikator asam basa.
Indikator asam basa adalah indikator yang bisa berubah warna akibat penambahan larutan asam maupun basa. Perubahan itu bersifat spesifik untuk masing-masing larutan.
- Suatu larutan dikatakan asam jika memiliki nilai pH < 7.
- Suatu larutan dikatakan basa jika memiliki nilai pH > 7.
Indikator asam basa dibedakan menjadi dua, yaitu indikator alami dan buatan.
1. Indikator Alami
Adalah indikator yang memanfaatkan bahan alami seperti kubis ungu, bunga kembang sepatu, bayam merah, dan sebagainya.
Contoh:
- Saat ditetesi larutan basa, kubis ungu akan berubah warna menjadi kehijauan.
- Saat ditetesi larutan asam, kubis ungu akan berubah warna menjadi merah muda.
2. Indikator buatan
Adalah indikator yang diproduksi oleh manusia, contohnya kertas lakmus, pH meter, pH meter digital, dan sebagainya.
Contoh:
- Saat ditetesi larutan asam, kertas lakmus biru akan berubah merah. Artinya, larutan asam bisa memerahkan lakmus.
- Saat ditetesi larutan basa, kertas lakmus merah akan berubah menjadi biru. Artinya, larutan basa bisa membirukan lakmus.
Agar semakin paham dengan klasifikasi materi, yuk simak contoh soal berikut.
Contoh Soal 1
Perhatikan beberapa benda berikut.
- Kayu
- Besi
- Alkohol
- Gas nitrogen
- Gas oksigen
Tentukan benda yang memiliki energi gerak partikel terbesar!
Pembahasan:
Energi gerak partikel dipengaruhi oleh jarak antarpartikel di dalam suatu benda. Semakin besar jarak antarpartikelnya, semakin besar energi geraknya.
Dari kelima benda yang disebutkan pada soal, benda yang jarak antarpartikelnya besar adalah gas nitrogen dan oksigen. Hal itu karena gas memiliki susunan partikel sangat renggang, sehingga partikelnya bebas untuk bergerak.
Jadi, benda-benda yang memiliki energi gerak partikel terbesar adalah gas nitrogen dan gas oksigen.
Contoh Soal 2
Perhatikan gambar berikut.
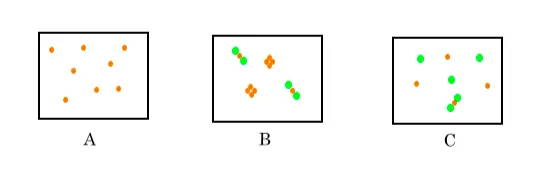
Analisislah gambar A, B, dan C tersebut apakah termasuk unsur atau molekul!
Pembahasan:
- Gambar A menunjukkan unsur. Hal itu karena terdapat atom-atom berwarna orange yang tidak saling berikatan.
- Gambar B menunjukkan molekul senyawa dan molekul unsur.
- Molekul unsur ditunjukkan oleh atom berwarna orange yang saling berikatan. (ikatan atom sejenis)
- Molekul senyawa ditunjukkan oleh atom berwarna orange dan hijau yang saling berikatan. (ikatan atom berlainan jenis)
- Gambar C menunjukkan dua unsur dan molekul senyawa.
- Dua unsur yang dimaksud ditunjukkan oleh atom hijau dan orange yang tidak saling berikatan.
- Molekul senyawa ditunjukkan oleh atom berwarna hijau dan orange yang saling berikatan.
Contoh Soal 3
Perhatikan tabel berikut.
| Larutan | Lakmus merah | Lakmus biru |
|---|---|---|
| P | merah | biru |
| Q | merah | merah |
| R | merah | biru |
| S | biru | biru |
Berdasarkan tabel di atas, tentukan kesimpulanmu!
Pembahasan:
Perhatikan kembali tabel pada soal.
- Larutan P
Saat ditetesi larutan P, lakmus merah tetap merah dan lakmus biru tetap biru. Artinya, larutan P bersifat netral atau pH = 7.
- Larutan Q
Saat ditetesi larutan Q, kertas lakmus merah tetap merah dan lakmus biru berubah menjadi merah. Artinya, larutan Q bersifat asam atau pH < 7.
- Larutan R
Saat ditetesi larutan R, lakmus merah tetap merah dan lakmus biru tetap biru. Artinya, larutan R bersifat netral atau pH = 7.
- Larutan S
Saat ditetesi larutan S, lakmus merah berubah menjadi biru dan lakmus biru tetap biru. Artinya, larutan S bersifat basa atau pH > 7.
Jadi, kesimpulannya adalah larutan P dan R bersifat netral, larutan Q bersifat asam, dan larutan S bersifat basa.

